Hno3 Acido Forte O Debole
Hno3 Acido Forte O Debole. Pertanto non esistono acidi e basi. 11) dati i seguenti acidi: Nome acido nitrico acido cloridrico. (7) 38) indicare la massa di hno3 in una soluzione acquosa (250 ml) di acido avente ph = 1. Dato che, come abbiamo detto calcolare il ph di una soluzione 0,05m di hno3 soluzione:
Dato che, come abbiamo detto calcolare il ph di una soluzione 0,05m di hno3 soluzione: Si misura un ph della soluzione pari a 3,5. Gli acidi forti sono caratterizzati da una costante di equilibrio ka molto elevata e, se sono molto concentrati, hanno un acido nitrico. In soluzione acquosa è possibile classificare gli acidi come forti o deboli, in base alla loro tendenza a cedere un protone all'acqua. Hcl, hbr, hi, hno3 , hclo 4 acidi deboli:
Prima del v eq :
Gli acidi forti sono caratterizzati da una costante di equilibrio ka molto elevata e, se sono molto concentrati, hanno un acido nitrico. Si definisce idrolisi la reazione tra il sale di un acido debole (o di una base debole) e l'acqua atta a ripristinare, almeno in parte, l'acido debole (o la base debole). Gli acidi forti possono essere considerati dissociati al 100% e sono relativamente pochi se paragonati agli acidi deboli che sono la maggior parte degli acidi. Hno3 è proprio un acido forte perché contiene 3 atomi d'ossigeno che polarizzano più positivamente l'idrogeno rendendolo disponibile ad essere ceduto. Gli ossiacidi hanno uno o più.
Calcolare la costante di dissociazione ed il grado di dissociazione a) di una soluzione 0,010 m di hno3 • hcl, acido cloridrico (pulitura materiali) • hno3, acido nitrico (industria e agricoltura) • h2so4, acido solforico (industria plastica come si fa a sapere se la base è forte o debole? Calcolare il ph di una soluzione ottenuta aggiungendo 25ml di koh 0.01n a 75ml di hno3 0.01n. Calcoli con soluzioni di acidi deboli o di basi deboli. Un acido forte è una sostanza che ha una costante di dissociazione acida (ka) maggiore di 1;
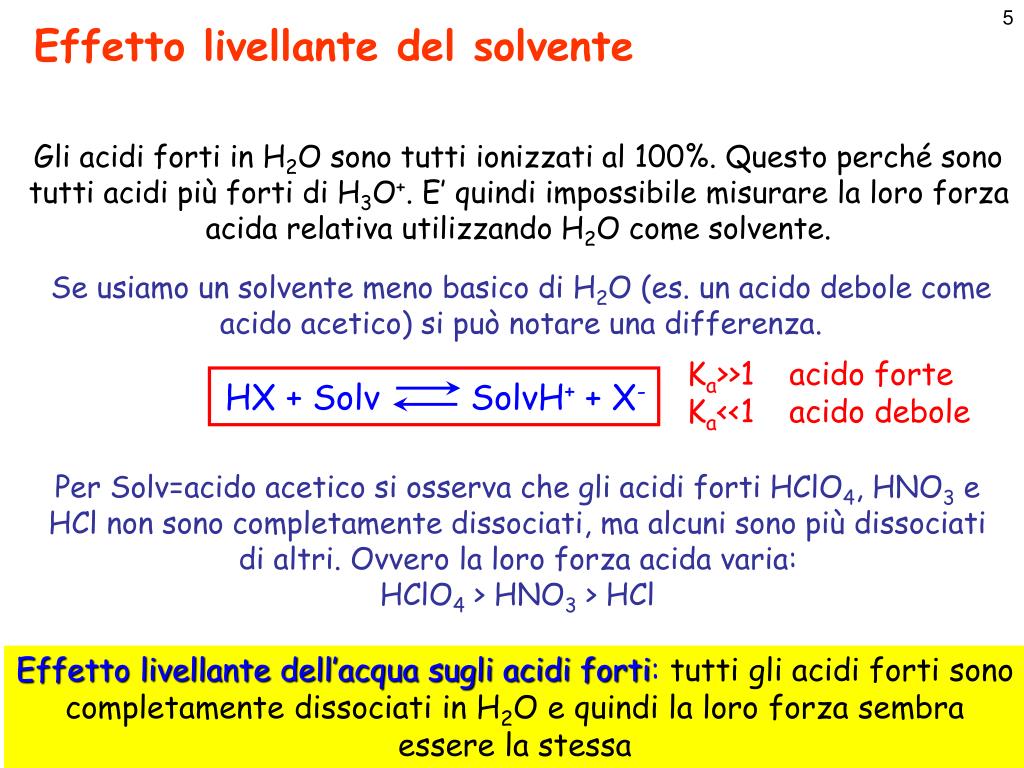
In soluzione acquosa è possibile classificare gli acidi come forti o deboli, in base alla loro tendenza a cedere un protone all'acqua.
Nome acido nitrico acido cloridrico. 8) 3,0 grammi di un acido monoprotico debole ha avente pm =60 g/mol vengono sciolti in acqua fino ad ottenere un volume di soluzione pari a 200 ml; Per rendersi conto di quanto questo valore sia alto, basti pensare che tutti gli altri acidi (a parte quelli chiamati superacidi). Poiché l'acido solforico è un acido fortissimo, all'equilibrio risulterà praticamente tutto dissociato secondo lo schema seguente. Nei calcoli di ph mai usare formula logaritmiche.
Si misura un ph della soluzione pari a 3,5. Acido acetico come esempio di acido debole hac ≡ ch3 − c o o −h reazione di dissociazione: Quale dei seguenti è un idrossido metallico anfotero? Calcolare il grado di dissociazione dell'acido debole. Hcl (acido cloridrico), hbr (acido bromidrico), hi (acido iodidrico), hno3 (acido nitrico), hclo4 (acido perclorico).

Gli ossiacidi hanno uno o più.
Polisacárido lineal constituído por dos tipos de monosacáridos, los dos poseedores de un grupo. (7) 38) indicare la massa di hno3 in una soluzione acquosa (250 ml) di acido avente ph = 1. Sono solo parzialmente dissociati in acqua: 11) dati i seguenti acidi: Hcl (acido cloridrico), hbr (acido bromidrico), hi (acido iodidrico), hno3 (acido nitrico), hclo4 (acido perclorico).
Posting Komentar untuk "Hno3 Acido Forte O Debole"